Chuẩn độ là một phương pháp phân tích định lượng chính xác, được áp dụng rộng rãi trong các ngành công nghiệp, nghiên cứu khoa học và kiểm tra chất lượng sản phẩm. Bài viết sẽ thông tin đến bạn các thao tác chuẩn độ cơ bản, giúp bạn hiểu rõ hơn về quy trình thực hiện và các bước cần thiết để đạt được kết quả chính xác.
Chuẩn độ là một kỹ thuật phân tích định lượng cơ bản và quan trọng trong hóa học, được sử dụng để xác định nồng độ của một chất phân tích trong dung dịch. Phương pháp này dựa trên nguyên lý cho dung dịch chuẩn có nồng độ đã biết vào dung dịch cần phân tích cho đến khi phản ứng hoàn toàn giữa hai chất. Để nhận biết điểm hoàn thành của phản ứng, người ta thường sử dụng chất chỉ thị, đây là chất có khả năng thay đổi màu sắc rõ rệt khi phản ứng đã đạt đến điểm tương đương.
Quá trình chuẩn độ không chỉ đơn giản mà còn mang lại độ chính xác cao, độ lệch chuẩn thường dưới 1%. Điều này phần nào cũng chứng tỏ độ tin cậy và tính nhất quán của phương pháp này. Chuẩn độ có thể được sử dụng để xác định nồng độ axit, bazơ, muối hay các chất oxi hóa khử khác trong các mẫu dung dịch.
Chuẩn độ có thể được phân loại theo phương pháp nhận biết điểm kết thúc hoặc theo loại phản ứng hóa học. Dưới đây là các loại chuẩn độ phổ biến:
Chuẩn độ axit-bazơ: Dùng để xác định nồng độ dung dịch acid hoặc bazơ với nguyên tắc dựa trên phản ứng trung hòa giữa ion H+ và OH-. Phương pháp này khá đơn giản và phổ biến trong phân tích hóa học.
Chuẩn độ oxy hóa khử: Sử dụng phản ứng oxy hóa khử giữa chất phân tích và dung dịch chuẩn độ để xác định nồng độ của chất phân tích.
Chuẩn độ tạo phức: Dùng để xác định độ cứng nước hoặc mức độ ion kim loại. Nguyên tắc là hình thành phức chất giữa dung dịch chuẩn độ và chất phân tích, với EDTA là chất thường dùng.
Chuẩn độ kết tủa: Phản ứng giữa dung dịch chuẩn độ và chất phân tích tạo thành muối không tan. Ví dụ là chuẩn độ bạc và chuẩn độ chất hoạt động bề mặt.
Chuẩn độ Karl Fischer: Dùng để xác định hàm lượng nước trong mẫu, sử dụng thuốc thử Karl Fischer. Phương pháp này chính xác và thường dùng trong các ngành như thực phẩm và dược phẩm.
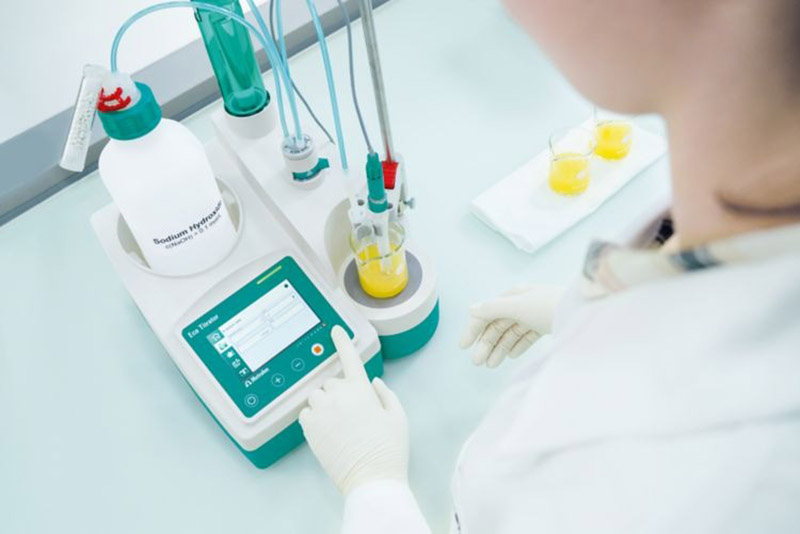
Nguyên tắc của chuẩn độ là xác định điểm tương đương hay còn gọi là điểm kết thúc của phản ứng, trong đó lượng chất phản ứng trong dung dịch chuẩn hoàn toàn phản ứng với chất cần xác định trong dung dịch phân tích. Điểm này được xác định thông qua sự thay đổi các tính chất vật lý hoặc hóa học của dung dịch, chẳng hạn như sự thay đổi pH hoặc sự thay đổi điện thế trong dung dịch.
Trong thực tế, khi thực hiện chuẩn độ axit-bazơ, điểm tương đương có thể được xác định thông qua thay đổi màu sắc của chất chỉ thị hoặc đo lường sự thay đổi pH. Tương tự, trong chuẩn độ oxy hóa-khử, điểm tương đương được xác định khi các ion trong dung dịch hoàn toàn phản ứng. Kết quả từ quá trình này sẽ cho phép tính toán chính xác nồng độ của chất phân tích trong dung dịch.
Một phép chuẩn độ bao gồm bốn bước chính sau:
Đầu tiên, dung dịch chuẩn độ cần được chuẩn hóa để xác định chính xác nồng độ, từ đó đảm bảo độ chính xác của kết quả chuẩn độ. Quá trình chuẩn hóa giúp cải thiện độ tin cậy và độ chính xác của phép đo.
Để thực hiện chuẩn độ, mẫu cần phải ở dạng dung dịch. Vì vậy, mẫu rắn sẽ được hòa tan hoặc xử lý trước (ví dụ như chiết xuất hoặc tro hóa) để giải phóng chất phân tích.
Trong một số trường hợp, dung dịch bổ trợ cũng cần được thêm vào. Chẳng hạn như chuẩn độ oxy hóa-khử thường yêu cầu điều chỉnh pH của dung dịch. Các phép chuẩn độ gián tiếp cũng luôn cần một dung dịch bổ trợ vì chất phân tích cần phải được chuyển đổi thành dạng có thể phản ứng sau đó mới được sử dụng trong quá trình chuẩn độ.
Đối với chuẩn độ ngược (hay chuẩn độ lượng dư), trước tiên, một lượng dư thuốc thử sẽ được thêm vào mẫu. Thuốc thử này phản ứng với chất phân tích và lượng dư của nó sẽ được chuẩn độ.
Trong quá trình chuẩn độ, mẫu cần được khuấy trộn để dung dịch chuẩn độ và chất phân tích được hòa trộn đều. Dung dịch chuẩn độ sẽ được thêm vào mẫu cho đến khi đạt điểm kết thúc.
Trong chuẩn độ thủ công, người ta thường sử dụng chất chỉ thị màu để xác định điểm kết thúc. Trong khi đó, các thiết bị chuẩn độ hiện đại sử dụng điện cực hoặc các cảm biến khác để phát hiện điểm tương đương. Thể tích dung dịch chuẩn độ được thêm vào sẽ được ghi lại cùng với tín hiệu đo, từ đó vẽ ra đường cong chuẩn độ.
Sau khi chuẩn độ hoàn tất, kết quả sẽ được tính toán. Nếu sử dụng thiết bị chuẩn độ tự động, nó sẽ tự động tính toán kết quả dựa trên các thông số cần thiết. Các biến số quan trọng trong phép tính bao gồm:
Kích cỡ mẫu (khối lượng hoặc thể tích mẫu).
Nồng độ dung dịch chuẩn độ (thường dùng đơn vị mol/L).
Titer (hệ số hiệu chỉnh dung dịch chuẩn độ).
Thể tích dung dịch chuẩn độ đến điểm kết thúc (mL).
Hệ số tỉ lệ phản ứng giữa chất phân tích và dung dịch chuẩn độ.
Dựa trên các biến số này, nồng độ chất phân tích có thể được tính toán bằng công thức phù hợp. Công thức tính có thể khác nhau tùy thuộc vào đơn vị kết quả và loại chuẩn độ thực hiện, đặc biệt là trong trường hợp chuẩn độ ngược.

Chuẩn độ là một phương pháp phân tích không thể thiếu trong nhiều lĩnh vực khoa học và công nghiệp. Một số ứng dụng nổi bật của chuẩn độ bao gồm:

Lời kết
Thao tác chuẩn độ dù là trong phòng thí nghiệm hay môi trường công nghiệp đều yêu cầu sự chính xác và cẩn thận. Việc nắm vững các bước thực hiện chuẩn độ sẽ giúp bạn có thể xác định nồng độ của chất phân tích một cách chính xác, từ đó ứng dụng vào nhiều lĩnh vực như kiểm tra chất lượng thực phẩm, dược phẩm hay nghiên cứu khoa học. Hy vọng bài viết này đã cung cấp cho bạn cái nhìn tổng quan về thao tác chuẩn độ và tầm quan trọng của nó trong các quá trình phân tích